Pengertian Benzena, Sifat, Struktur dan Contohnya
Dalam dunia kimia organik, benzena merupakan senyawa aromatik yang sangat penting dan banyak digunakan di berbagai industri. Senyawa ini dikenal karena struktur cincin heksagonalnya yang khas serta kestabilannya yang tinggi. Benzena menjadi bahan dasar dalam pembuatan berbagai produk, mulai dari plastik hingga obat-obatan.
Sebagai seorang profesional di laboratorium, memahami struktur, sifat, dan reaktivitas benzena sangatlah penting. Artikel ini akan mengulas secara lengkap pengertian benzena, sifat fisika dan kimianya, struktur resonansi, hingga contoh penggunaan dalam kehidupan sehari-hari.
Pengertian Benzena
Benzena adalah senyawa hidrokarbon aromatik dengan rumus molekul C₆H₆. Senyawa ini terdiri dari enam atom karbon yang tersusun dalam struktur cincin planar (heksagonal), masing-masing terikat pada satu atom hidrogen. Keunikan benzena terletak pada sistem ikatan rangkap terdelokalisasi di dalam cincin karbonnya.

Benzena pertama kali ditemukan oleh Michael Faraday pada tahun 1825 dalam gas yang dihasilkan dari pencairan minyak lampu. Kemudian, August Kekulé mengusulkan struktur cincin benzena pada tahun 1865 yang menjadi dasar bagi pemahaman modern mengenai senyawa aromatik.
Struktur Benzena
Struktur benzena sangat unik karena ikatan rangkap tidak terlokalisasi seperti pada alkena biasa. Sebaliknya, enam elektron π (pi) dari ikatan rangkap tersebar merata di atas dan di bawah cincin karbon. Hal ini menciptakan stabilitas ekstra yang disebut aromaticity (aromatisitas).
Diagram struktur benzena dapat digambarkan sebagai berikut:
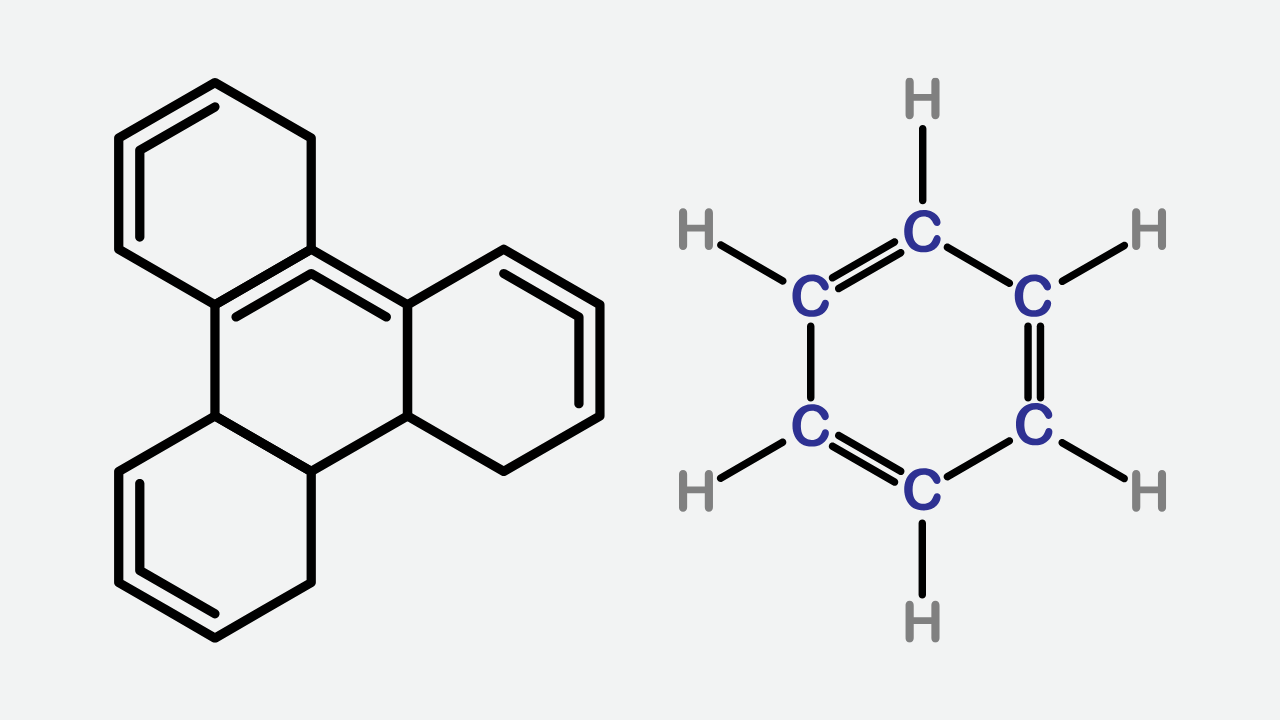
Namun, dalam kenyataannya, struktur ini tidak memiliki ikatan rangkap tetap. Seluruh ikatan C–C dalam cincin benzena memiliki panjang yang sama, yaitu sekitar 1,39 Å — panjang ini berada di antara panjang ikatan tunggal (1,54 Å) dan ikatan rangkap (1,34 Å).
Rumus Kimia dan Struktur Resonansi
- Rumus molekul: C₆H₆
- Struktur resonansi: Benzena memiliki dua bentuk resonansi yang setara. Kedua struktur ini terus-menerus bergantian secara teoritis dan tidak dapat dipisahkan dalam bentuk nyata.
Struktur resonansi ini menjelaskan kestabilan ekstra yang dimiliki benzena dibandingkan alkena siklik lainnya.
Sifat-Sifat Benzena
1. Sifat Fisika
- Wujud: Cairan tidak berwarna
- Titik didih: 80,1 °C
- Titik leleh: 5,5 °C
- Bau: Aromatik khas
- Kelarutan: Tidak larut dalam air, tetapi larut dalam pelarut organik seperti eter dan alkohol
2. Sifat Kimia
- Benzena tidak mengalami reaksi adisi seperti alkena karena kestabilan sistem aromatiknya.
- Reaksi utama benzena adalah reaksi substitusi elektrofilik aromatik, misalnya:
- Nitrasi: menghasilkan nitrobenzena
- Halogenasi: menghasilkan bromobenzena atau klorobenzena
- Sulfonasi: menghasilkan asam benzenasulfonat
- Alkilasi (reaksi Friedel-Crafts): menghasilkan senyawa alkilbenzena
Contoh Penggunaan Benzena
Benzena merupakan bahan baku penting dalam industri kimia. Berikut beberapa contoh penggunaannya:
- Produksi Styrene: Benzena diubah menjadi etilbenzena, lalu diolah menjadi styrene yang digunakan untuk membuat plastik polistirena.
- Pembuatan Anilin: Benzena diubah menjadi nitrobenzena, lalu direduksi menjadi anilin, bahan baku untuk zat warna.
- Pembentukan Fenol: Benzena diubah menjadi fenol melalui proses oksidasi.
- Zat aditif bahan bakar: Beberapa senyawa turunannya digunakan untuk meningkatkan angka oktan bahan bakar.
Bahaya Benzena bagi Kesehatan
Meskipun sangat berguna, benzena juga tergolong sebagai zat karsinogenik (penyebab kanker). Paparan berkepanjangan terhadap uap benzena dapat menyebabkan:
- Kerusakan sumsum tulang
- Penurunan jumlah sel darah putih (leukopenia)
- Leukemia
- Iritasi pada kulit dan saluran pernapasan
Oleh karena itu, penanganan benzena harus dilakukan dengan alat pelindung dan prosedur keselamatan laboratorium yang ketat.
Kesimpulan
Benzena merupakan senyawa aromatik yang sangat stabil dan penting dalam kimia organik serta industri modern. Struktur resonansi dan sifat kimianya yang khas menjadikan benzena sebagai dasar dari banyak senyawa aromatik lainnya. Namun, penggunaannya juga menuntut kehati-hatian karena sifat toksiknya.
Sebagai ahli laboratorium atau pelajar kimia, pemahaman mendalam tentang benzena tidak hanya meningkatkan pemahaman teoritis, tetapi juga mendukung penerapan yang aman dalam praktik kimia.
FAQ tentang Benzena
Mengapa benzena lebih stabil dibandingkan senyawa alkena biasa?
Karena benzena memiliki sistem ikatan pi yang terdelokalisasi di seluruh cincin karbonnya, menciptakan energi resonansi yang membuat struktur aromatiknya sangat stabil.
Apa itu reaksi substitusi elektrofilik aromatik?
Ini adalah jenis reaksi kimia di mana atom hidrogen pada cincin benzena digantikan oleh gugus lain (seperti NO₂, Cl, atau CH₃) melalui mekanisme elektrofilik, tanpa menghancurkan sistem aromatiknya.
Apakah benzena terdapat secara alami?
Ya, benzena dapat ditemukan secara alami dalam gas vulkanik, asap kebakaran hutan, serta sebagai komponen dalam minyak mentah.
Apa bedanya benzena dengan senyawa aromatik lain?
Benzena adalah senyawa aromatik paling sederhana dan menjadi acuan utama dalam klasifikasi senyawa aromatik lainnya yang memiliki sistem ikatan pi terkonjugasi dalam cincin.