Ikatan logam dan sifat-sifatnya

Drude dan Lorentz mengemukakan model, bahwa logam sebagai suatu kristal terdiri dari ion-ion positif logam dalam bentuk bola-bola keras dan sejumlah elektron yang bergerak bebas dalam ruang antara. Elektron-elektron valensi logam tidak terikat erat (karena energi ionisasinya rendah), sehingga relatif bebas bergerak. Hal ini dapat dimengerti mengapa logam bersifat sebagai penghantar panas dan listrik yang baik, dan juga mengkilat. Gambar 1 berikut mengilustrasikan suatu model logam dengan elektron-elektron membentuk suatu “lautan” muatan negatif.
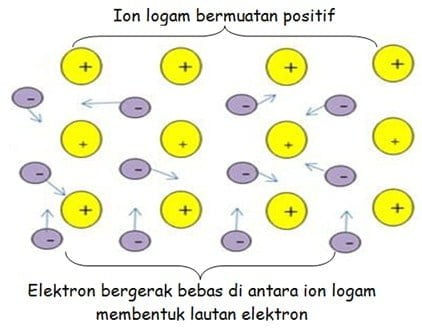
Model lautan elektron ini sesuai dengan sifat-sifat logam, seperti: dapat ditempa menjadi lempengan tipis, ulet karena dapat direntang menjadi kawat, memiliki titik leleh dan kerapatan yang tinggi. Logam dapat dimampatkan dan direntangkan tanpa patah, karena atom-atom dalam struktur kristal harus berkedudukan sedemikian rupa sehingga atom-atom yang bergeser akan tetap pada kedudukan yang sama. Hal ini disebabkan mobilitas lautan elektron di antara ion-ion positif meru-pakan penyangga (Gambar 1).
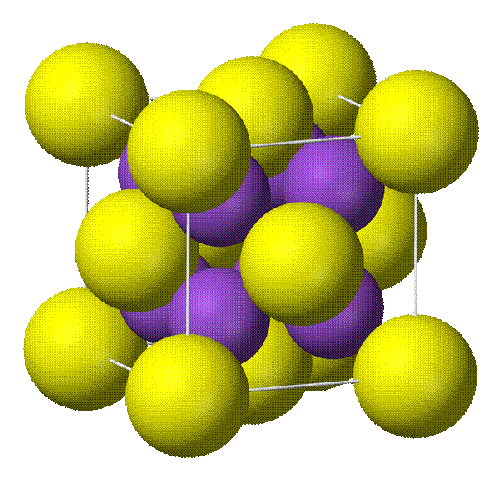
Keadaan yang demikian ini berbeda dengan kristal ionik. Dalam kristal ionik, misalnya NaCl, gaya pengikatnya adalah gaya tarik menarik antar ion-ion yang muatannya berlawanan dengan elektron valensi yang menempati kedudukan tertentu di sekitar inti atom. Bila kristal ionik ini ditekan, maka akan terjadi keretakan atau pecah. Hal ini disebabkan adanya pergeseran ion positif dan negatif sedemikian rupa sehingga ion positif berdekatan dengan ion positif dan ion negatif dengan ion negatif, keadaan yang demikian ini mengakibatkan terjadi tolak-menolak sehingga kristal ionik. menjadi retak (gambar 2)
Perbandingan sifat-sifat fisis logam dengan non logam ditabulasikan berikut.
Tabel. Perbandingan sifat-sifat fisis logam dengan non logam